Des semaines cruciales pour Ablynx et Bone Therapeutics
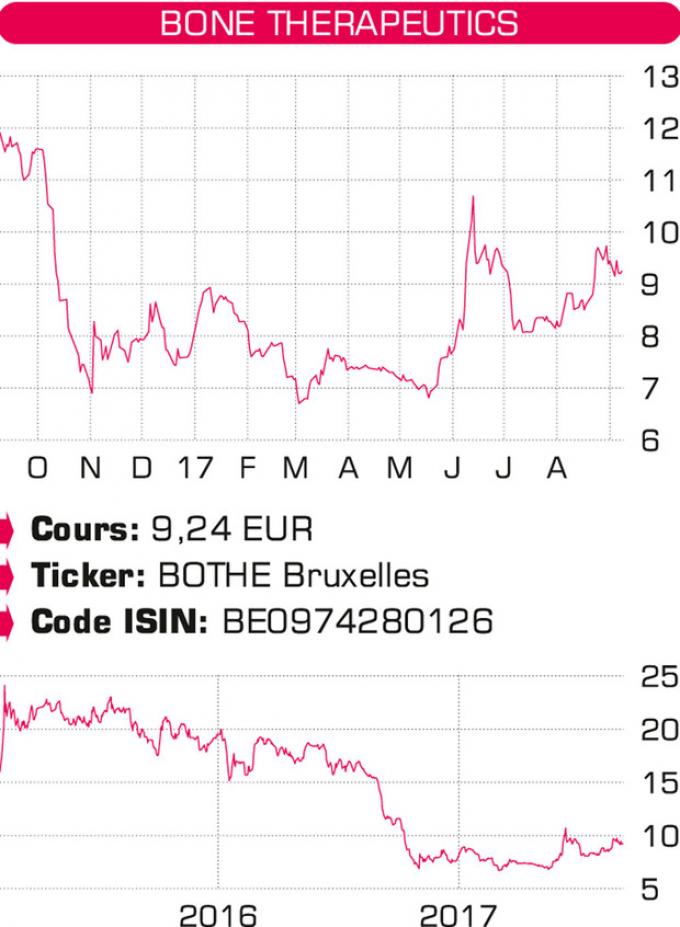
Source: Newsgate
3 min. de lecture
Vous avez repéré une erreur ou disposez de plus d’infos? Signalez-le ici